Coordination Chemistry §1 錯体化学の基礎 1 金属錯体とは 2 金属錯体の構造 3 金属錯体の異性現象 4 化学式と命名法2 25mLメスフラスコ8本を用意し、ビュレットを用いて1で調製した混合 溶液を1、2、3、4、5、10、15、mLを加え、定容する. 吸収スペクトル測定 1 分光光度計のセットアップ:「分光光度計の使用法」→「測定前の準着色鉄錯体の調製 鉄含有量の比色定量には、3分子の1,10フェナントロリン(オル トフェナントロリンとも呼ばれる、またはphenと略される)が第 一鉄イオン(Fe2)と錯体を形成することを利用します。 FL ˜ ˚ ˛ ˝ ˙ ˆ ˇ ˘ 図1 1,10フェナントロリンの

18 1099号 銅錯体溶液とその製造方法 Astamuse
1 10-フェナントロリン 鉄 錯体 最大吸収波長
1 10-フェナントロリン 鉄 錯体 最大吸収波長-鉄イオン は,3分子の1,10フェナントロリンと錯体を形成する。配位結合は1,10フェナントロリンの2個の 窒素との間で生じる。この時の鉄イオンは,d2sp3浬成軌道による正八面体構造(双四角錐型,双ピラ ミッド型)の配位をする。ラーセンサーであり,Red の波長域は575~660 nm(最大 感度波長615 nm),Green の場合は455~630 nm(530 nm),Blue の場合は400~540 nm(460 nm)である.Fig 1 に示すように,分光光度計U5100 で測定した1,10フェナ ントロリン-鉄錯体の吸収極大波長は510 nm である.570



2
フェロイン (英 ferroin) は、化学式 Fe(ophen) 3SO 4 で表される有機化合物である。 ophen は二座配位子である1,10フェナントロリン (C 12 H 8 N 2) の略である。「フェロイン」という言葉は塩化物など幅広いアニオンとの塩に対して使われる。鉄(II)イオンとoフェナントロリンの1:3錯体 は濃赤色で,微量の鉄(II)イオンの検出に利用され, またこの濃赤色は鉄(III)錯体になるとあざやかに 変色(淡青色)するので,酸化還元指示薬(フェロ イン)として用いられる16。なお,ophen配位子S-1 となり,約00 倍の速度の増大が確認された。この接触 作用をFIA システムに導入したところ,銅01~10 ng ml-1 を自動計測することができた8)。銅イオンの触媒サイクルを図 1 に示す。図 1 のようにphenの代わりに,2,4,6 トリス(2
*3 1,10フェナントロリンは酸性条件では酸型になり鉄と錯体を作らなくなるので、pHの設定(pH 3~9)には注意が必要である。 *4 わずかながら1,10フェナントロリンは510 nmに吸収を示すので、鉄を入れない場合の吸光度を差し引く必要がある。LambertBeerの法則 3 LambertBeerの法則 ※希薄溶液のみに成り立つ A 吸光度 (無次元量) ε モル吸光係数 (L・mol–1・cm–1) c 溶質のモル濃度 (mol・L–1) d 吸収層の厚さ(セル長) (cm) ※モル吸光係数εは 波長ごとに異なるMembrane Substances 0000 title abstract 4;
1,10フェナントロリン textskipToContent textskipToNavigation お客様のニーズに合ったより良いサービスを提供するために、当ウェブサイトではCookieを使用しています。この錯体が光を吸収し、電極上に電子を渡す。効 率はシリコンなどの太陽電池には劣るとか、耐久性に問題があるなどの課題があるが、実用に近い状況で研究されてい る。 公開特許公報 1 10フェナントロリン 鉄 錯体 最大吸収波長Discuss1 1,10phenanthroline metal complex Chemical class 0000 title claims description 28;
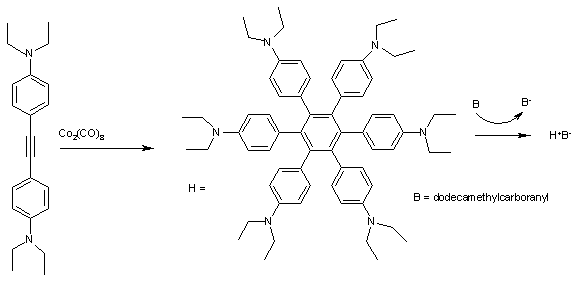



電荷移動錯体 Wikipedia



2
Application Note No 1 2 蛍光の原理 光の波長と種類 光は波長によって表現され、赤外線・可視光線・紫外線に分類されます。 波長は、紫外線 1~400nm、可視光線 380~800nm、赤外線 800nm~1000nm の範囲となります。 波長 光は波長として表現できます。Coordination Chemistry 電子吸収スペクトル l (光路長) I 0 I E = hν= hc/λ c (濃度) 紫外・可視・近赤外線 透過度: ΔS = 0 吸光度:A = log I 0 /I = εcl LambertBeerの法則 モル吸光係数:ε M1 cm1 錯体は様々な電子状態(項・term)をとるFe(II)の1,10フェナントロリン錯体のモル吸光係数を調べています。「分析化学辞典」や「金属キレート」等の書籍を一通りあたってみたのですが、見つけることができませんでした。インターネットで探してみると、 化学 締切済 教えて!goo




10 号 金属材料の簡易成分分析方法 Astamuse



酸素分子検出方法 酸素分子検出プローブおよびバイオイメージング方法
1透過率t:ある波長の光が溶液層を通過したと き,入射光の強度と透過光の強度の比で表したものであ る。ここで,透過前の強度を1 とした場合の透過後の 強度を透過率t と呼ぶ。この透過率に100 をかけた値 が透過率パーセント%t である。鉄 鉄1000gをビーカーに採り、少量の硝酸(11)を加えて加熱溶解し、冷後、メスフ ラスコに移し、硝酸(1160)を加えて1Lとしたもの。 銅 銅1000gをビーカーに採り、少量の硝酸(11)を加えて加熱溶解し、冷後、メスフチオシアナト鉄(iii)錯体、1,10フェナントロリン鉄(ii)錯体および銅(i)錯体などはこの例で、前者では から へ電子が移動して 基と を生成し、後者では金属の 電子が配位子の 軌道へ移動します。




Pdf Fundamental Knowledge Of Chemical Analysis Spectrophotometry



フェナントロリン吸光光度法によるの鉄の定量
Tris (1,10phenanthroline)ruthenium (II) Bis (hexafluorophosphate) ・川口,尼崎倉庫の在庫は即日,その他の倉庫は2〜3営業日以内の出荷となります。 川口,尼崎倉庫からの配送対象エリア は各々異なります。 納期に関するご質問は営業部までお問い合わせください原理 測定試料に1,10−フェナントロリン溶液を加え,生成しただいだい赤の錯体を波長510nmで 定量する。全鉄又は全溶存鉄を定量 する −1,10−フェナントロリン錯体はpH25〜9で安定であり 7113 吸収化合物の生成 7112の溶液に1,10−比色試薬/金属指示薬 製品コード P007 oPhenanthroline CAS番号 化学名 1,10Phenanthroline, monohydrate 分子式・分子量 C 12 H 8 N 2 ・H 2 O=192



2



2
ALCLa錯体はF-が存在すると混合配位子錯体を形成し て、6nm付近に吸収極大を与える。この反応はF -に特 異的であり、F-の定量法として優れている。しかし、ALCLa錯体をALCから調製するには手間がかかり、調製法のこの実験は、鉄(Ⅱ)イオンFe2+が1,10 -フェナントロリンと反応して、 Fe2+:phen=1:3の金属キレートを生成する反応を利用している。 この金属錯体は長時間変化せず安定で、1,10 -フェナントロリンと錯体を形成するのは 2価の鉄のみである。図 24 鉄の濃度 00、10、、30、40 µg/mL における、鉄フェナントロリン錯体の吸収スペクトル。 図 25 鉄フェナントロリン錯体の510 nmにおける吸光度の検量線。




ポリ塩化ビニル膜を用いる比色定量法 利用統計を見る
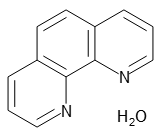



5144 8 1 10 フェナントロリン一水和物 1 10 Phenanthroline Monohydrate 161 169 詳細情報 常用試薬 ラボウェア 試薬 富士フイルム和光純薬
性質 1, 10フェナントロリン−水和物は,次の性質を示す。 (1) 性状 1, 10フェナントロリン−水和物は,白い結晶又は結晶性粉末で,エタノールに溶けやすく,水 及びジエチルエーテルに溶けにくい。 (2) 定性方法 試料の赤外吸収スペクトルをJIS K 0117にPolymerization reaction Methods 0000 claims abstract description 24;錯体(図の最後から2 番目)などの光を吸収する分子がつけてある。この錯体が光を吸収し、電極上に電子を渡す。効 率はシリコンなどの太陽電池には劣るとか、耐久性に問題があるなどの課題があるが、実用に近い状況で研究されてい る。




電荷移動錯体 Wikiwand



2
Coordination complex Chemical class 0000 claims abstract description 12;フェナントロリンの性質の一部は2,2'ビピリジン(英語版)と似ている。 1,10フェナントロリンの鉄 錯体はフェロイン (ferroin) と呼ばれ、電位の酸化還元指示薬(標準酸化還元電位 E 0 = 106 V) として滴定分析、吸光光度分析に用いられる試薬である。 合成3・1 吸収曲線 phen は鉄(II)と13の組成比を持つ赤色のキレート 錯体(Fe(phen) 3 2+)を生成し,吸収極大波長は510 nm 付近に存在する.その波長におけるモル吸光係数の値は 11×104 dm3 mol-1 cm-1 である14).JIS 法のFe(phen) 3 2+



2価の鉄イオンと1 10 フェナントロリンの錯体の構造式を教えて Yahoo 知恵袋



ブルー銅モデル錯体を酸化還元対に用いた色素増感型太陽電池
1.吸収スペクトル 波長vs吸光度 2.1,10フェナントロリン塩酸塩を用いて,溶液を調製 最終濃度が 4x10−4 M になるように,メスフラスコに採取 3.CH 3 COOH-CH 3 のとき錯体の生成量は最大1,10phenanthroline)をはじめとするビスフェ ナントロリン銅(I)錯体は、可視域に金属・配 位子電荷移動(MLCT)遷移に帰属される強 い吸収と燐光を示し、光触媒や太陽電池の光 増感剤などの光化学的な応用面で注目されて いる。重要な例として、鉄(Ⅱ)と1,10フェナントロリンのキレートがあげられる。 電荷移動遷移錯体のモル吸光係数は非常に大きく、εの値は一般的に cm 1 mol 1 Lである。



2




Fe Ii の1 10 フェナントロリン錯体のモル吸光係数を教えて下さい 化学 締切済 教えて Goo
今回、希土類錯体Eu(phen)2(NO3)3の粉末状態における発光量子収率の測 定を行いました。 結果として、1,10フェナントロリン(Phen)を直接励起し、ユーロピウム(Eu)の発 光量子収率として約08が得られました。Phenの発光が観測されないことから、図4.従来の主なEu(III)錯体の構造と性質. Type 1のEu(III)錯体は、大きな縮合環である1, 10フェナントロリンの影響で媒体に対する溶解性 が極めて小さい。一方、Type 2 のEu(III)錯体は、光吸収効率が小さいため十分な蛍光強度を得る ことができない。



1 10 フェナントロリン錯体による鉄の定量の実験の時の操作でわからないこ Yahoo 知恵袋



Fe測定方法について 血清鉄測定用 セロテック Fe L 製品案内 株式会社セロテック



公開特許公報



フェナントロリン吸光光度法によるの鉄の定量




21 号 発光素子 照明装置 発光装置 表示装置および電子機器 Astamuse



Fe測定方法について 血清鉄測定用 セロテック Fe L 製品案内 株式会社セロテック



3回生実験のこと 光吸収 1 2



特許 知財ポータル Ip Force




Jpwoa1 過酸化水素製造方法 過酸化水素製造用キットおよび燃料電池 Google Patents



特許 知財ポータル Ip Force




18 1099号 銅錯体溶液とその製造方法 Astamuse



2




08 号 酸素分子検出方法 酸素分子検出プローブおよびバイオイメージング方法 Astamuse



Fe測定方法について 血清鉄測定用 セロテック Fe L 製品案内 株式会社セロテック



甲南大学理工部機能分子科化学科 環境計測のための機器分析法




紫外 可視分光光度計による飲料中の鉄の濃度計算 Manualzz



特許 知財ポータル Ip Force




画像 鉄 フェナントロリン 錯体 モル吸光係数 鉄 フェナントロリン 錯体 モル吸光係数 Mbaheblogjpzd68



2
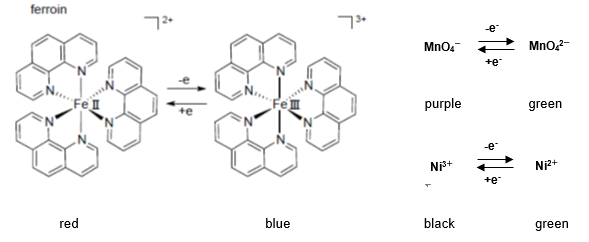



3分でわかる技術の超キホン エレクトロクロミズムとは 色変化の例や注目の用途を解説 アイアール技術者教育研究所 製造業エンジニア 研究開発者のための研修 教育ソリューション




フェナントロリン Wikipedia



2
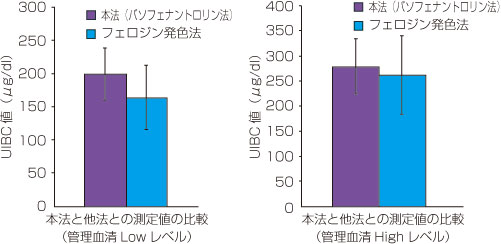



不飽和鉄結合能 Uibc の定量用キット マイクロアッセイuibc 不飽和鉄結合能 測定キット フナコシ



2




比色試薬 金属指示薬 Nitroso Psap 同仁化学研究所




フェナントロリン Wikiwand




Iv 鉄の定量とタンパク質の分析 実験 東京大学教養学部基礎化学実験オフィシャルページ



2



2



2




遷移金属錯体の色と発光



2価の鉄イオンと1 10 フェナントロリンの錯体の構造式を教えて Yahoo 知恵袋



2



2



特開18 知財ポータル Ip Force



2



Chap6 03
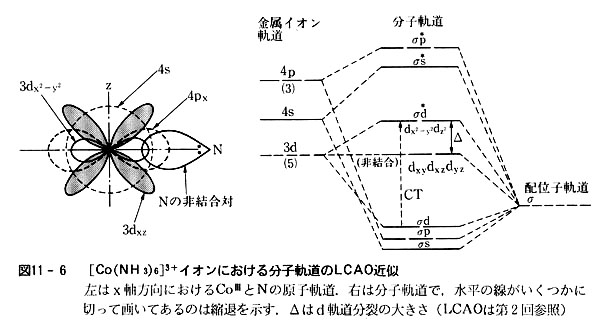



3 錯体の性質と配位結合



2




三元錯体生成反応系を利用する生体関連物質の吸光光度法の開発に関する研究
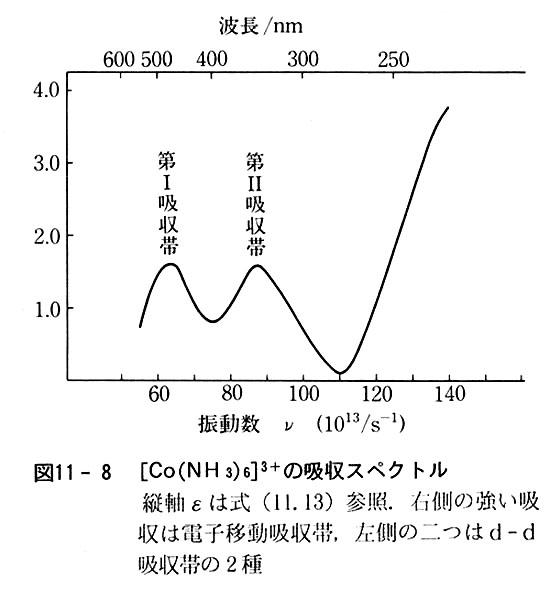



3 錯体の性質と配位結合
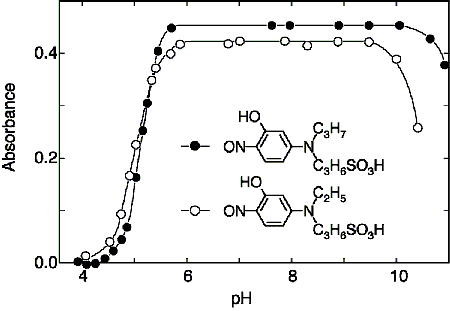



比色試薬 金属指示薬 Nitroso Psap 同仁化学研究所



2



2



2



2



フェナントロリン吸光光度法によるの鉄の定量




09 号 分光法のための分子色素 Astamuse



2



2



特許 知財ポータル Ip Force




号 ディスプレイデバイスで使用するためのbodipy化合物 Astamuse



2



2



フェナントロリン吸光光度法によるの鉄の定量



2




5144 8 1 10 フェナントロリン一水和物 1 10 Phenanthroline Monohydrate 161 169 詳細情報 常用試薬 ラボウェア 試薬 富士フイルム和光純薬



2



化学実験で 配位子の異なるコバルト錯体3つについて 紫外線可視吸収ス Yahoo 知恵袋



クロム マンガン 鉄 水浄化フォーラム 科学と技術



3



2



クロム マンガン 鉄 水浄化フォーラム 科学と技術



フェナントロリン吸光光度法によるの鉄の定量




至急お願いいたします 化学 画像の物質は1 10 フェナントロリン錯体の Okwave




13 号 医療用一酸化炭素放出レニウム化合物 Astamuse



2



フェナントロリン吸光光度法によるの鉄の定量



2



2



2



フェナントロリン吸光光度法によるの鉄の定量



2




Jpa 酸素分子検出方法 酸素分子検出プローブおよびバイオイメージング方法 Google Patents




Jpwoa1 有機金属錯体 有機el素子及び有機elディスプレイ Google Patents




16 号 重合体 前記重合体を有する光音響イメージング用造影剤 Astamuse



フェナントロリン鉄錯体の構造を教えてください フェナントロリンはベン Yahoo 知恵袋
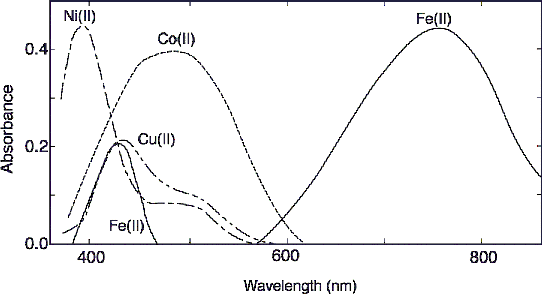



比色試薬 金属指示薬 Nitroso Psap 同仁化学研究所
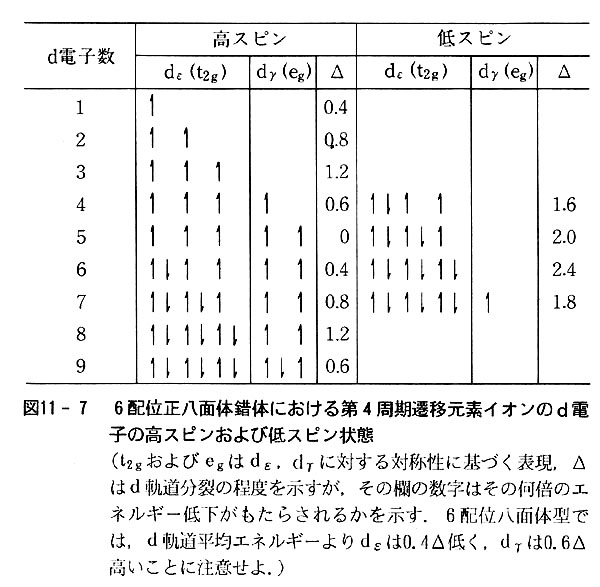



3 錯体の性質と配位結合



Fe測定方法について 血清鉄測定用 セロテック Fe L 製品案内 株式会社セロテック




07 号 光学記録媒体 光記録材料および金属錯体化合物 Astamuse



2



Fe測定方法について 血清鉄測定用 セロテック Fe L 製品案内 株式会社セロテック



2



2



0 件のコメント:
コメントを投稿